Guía Médica
The New York Times.
La Administración de Alimentos y Medicamentos (FDA) de EE.UU. aprobó el martes la primera prueba rápida para el coronavirus que se puede realizar en casa, y que arroja resultados en 30 minutos.
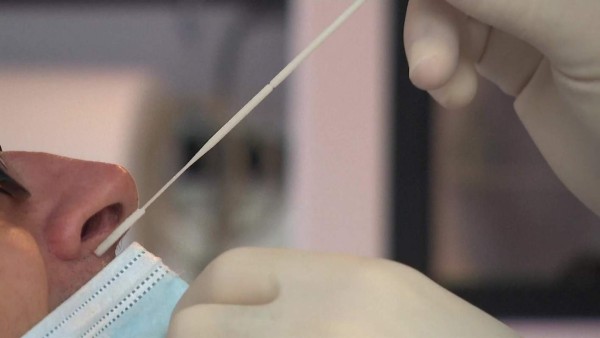
La sencilla prueba de frotis nasal, que fue desarrollada por Lucira Health, requiere una receta, y las personas menores de 14 años no pueden realizar la prueba en sí mismas, apuntó la FDA en una declaración.
La compañía de California dijo que los ensayos clínicos mostraron que un 100 por ciento de los pacientes pudieron realizar la prueba de Lucira en unos dos minutos. Esto es significativamente más rápido que los laboratorios, que ahora tardan de dos a siete días para generar los resultados de las pruebas, anotó la compañía en una declaración. La prueba costará unos 50 dólares.
La Administración de Alimentos y Medicamentos (FDA) de EE.UU. aprobó el martes la primera prueba rápida para el coronavirus que se puede realizar en casa, y que arroja resultados en 30 minutos.
La sencilla prueba de frotis nasal, que fue desarrollada por Lucira Health, requiere una receta, y las personas menores de 14 años no pueden realizar la prueba en sí mismas, apuntó la FDA en una declaración.
La compañía de California dijo que los ensayos clínicos mostraron que un 100 por ciento de los pacientes pudieron realizar la prueba de Lucira en unos dos minutos. Esto es significativamente más rápido que los laboratorios, que ahora tardan de dos a siete días para generar los resultados de las pruebas, anotó la compañía en una declaración. La prueba costará unos 50 dólares.
LEA: Vacuna de AstraZeneca arroja resultados alentadores
Hasta que Lucira acelere la fabricación de la pruebas solo estará disponible de forma limitada en los puntos de atención y las redes de atención de la salud que receten la prueba para que los pacientes las usen en casa, apuntó la compañía.
La compañía planifica enmendar o presentar una nueva solicitud de uso de emergencia en el segundo trimestre de 2021, de forma que las personas que piensen que tienen una infección con la covid-19 puedan comunicarse con un profesional médico en línea a través de un sitio web dedicado para gestionar una receta y la entrega durante la noche del kit de la prueba.
'La autorización de hoy de una prueba completa para realizar en casa es un paso significativo para la respuesta nacional de la FDA ante la COVID-19', comentó en una declaración Jeff Shuren, director del Centro de Dispositivos y Salud Radiológica de la FDA. 'Ahora, más estadounidenses que quizá hayan contraído la COVID-19 podrán tomar medidas inmediatas, basándose en sus resultados, para protegerse a sí mismos y a los que los rodean'.
Varias pruebas más han recibido la autorización de la FDA para la recolección de las muestras en casa, pero todas deben ser enviadas a un laboratorio para su procesamiento, reportó el The New York Times.
Las pruebas de laboratorio del material genético específico del coronavirus, que utilizan una técnica llamada reacción en cadena de la polimerasa (RCP), siguen siendo consideradas el estándar de excelencia para detectar al virus. Pero las nuevas pruebas para realizar en casa se basan en unos principios similares. Como la RCP, la nueva prueba copia de forma repetitiva el material genético hasta que alcanza unos niveles detectables. Aunque es más rápida y fácil de usar que las pruebas de RCP, en general se piensa que el nuevo método es menos preciso, reportó el Times.
Las personas que toman la prueba, que funciona con pilas, introducen un hisopo nasal en ambas orificio de la nariz, y luego introducen y agitan los hisopos en un frasco de sustancias químicas. Entonces, ese frasco se conecta con un cartucho de prueba que procesa a la muestra. En cuestión de media hora, el cartucho de prueba se iluminará con un resultado 'positivo' o 'negativo'. Las directrices federales anotan que las personas que tomen las pruebas deben reportar los resultados a sus proveedores de atención de la salud, que deben entonces informar a las autoridades de salud pública para ayudar a monitorizar la propagación del virus.
Una prueba del virus en casa 'tenía que suceder', declaró al Times Omair Garner, microbiólogo clínico y experto en diagnósticos del Sistema de Salud de la Universidad de California, en Los Ángeles. 'Tengo la esperanza de que funcione bien'.
Según Lucira, la prueba detectó de forma precisa un 94 por ciento de las infecciones encontradas por una prueba de RCP bien establecida. También identificó de forma correcta al 98 por ciento de las personas sanas sin infectar.
Pruebas de emergencia
Saskia Popescu, experta en prevención y epidemióloga de la Universidad de George Mason, en Virginia, advirtió que las pruebas en casa, aunque son un avance notable, no deben considerarse como una solución. Popescu dijo al Times que, para solventar las lagunas en el diagnóstico del coronavirus, 'necesitamos más pruebas basadas en laboratorio accesibles y rápidas'.
Unas vacunas contra la COVID se acercan a la aprobación del uso de emergencia
Pfizer y la firma alemana BioNTech anunciaron el jueves que su vacuna tiene una efectividad del 95 por ciento, y que solicitarán la aprobación para el uso de emergencia 'en cuestión de días'.
La vacuna experimental ya se había mostrado promisoria en un análisis inicial que se anunció la semana pasada, pero el ensayo se completó a una velocidad mayor de lo previsto debido al pico en los casos de coronavirus en Estados Unidos.
Los resultados del ensayo, que se entregaron menos de un año después de que los investigadores comenzaran a trabajar en la vacuna, rompieron todos los récords de velocidad respecto al desarrollo de una vacuna, reportó el Times.
La eficacia de la vacuna fue constante en los distintos grupos de edad, raza y etnia, según las compañías. El evento adverso más común fue la fatiga, ya que un 3.7 por ciento de los voluntarios reportaron cansancio tras recibir la segunda dosis. Un 2 por ciento de los voluntarios reportaron dolor de cabeza tras la segunda dosis. Los adultos mayores reportaron menos efectos secundarios, y unos efectos secundarios más leves, anotaron las compañías.